Sua professora não está completamente errada (bastante errada sim, mas não completamente). Essa história que você ouviu na escola de que a água tem somente três fases, a de vapor, a líquida e a sólida é só uma simplificação. Na verdade existem város tipos diferentes de gelo e mais uma fase amorfa, isto é, algo como um "vidro de gelo", um gelo líqüido. Dependendo da temperatura e da pressão você vai encontrar H
2O de um jeito diferente.
Você já deve alguma vez ter visto um diagrama de fases, se não vai uma pequena revisão:
Esse aqui é o diagram de fases da água que você conhece:

O lado laranja é o gelo com que estamos acostumados, o lado violeta é a nossa água líqüida e o lado verde é o vapor de água. Os pontos localizados nas interfaces entre essas regiões contêm uma mistura das duas fases. As setas representam transições de fase. Temos também dois pontos especiais, o ponto triplo, que contém uma mistura de três fases e o ponto crítico, que representa que para temperaturas além dele, não importa o quanto aumentemos a pressão, o vapor não pode mais ser transformado em água líqüida.
Só que o diagrama aí de cima não está completo, ele é só um pedacinho de um diagrama maior e mais complexo, tente encontrá-lo no meio do diagrama completo:

Está vendo a letra E perto da palavra "Solid"? Ela representa condições de pressão e temperatura habituais, são mais ou menos pressão e temperatura ambiente. Repare que para a pressão ambiente existem três tipos de gelo (trace uma linha horizontal a partir do E e verá), o gelo I
h, o I
c e o gelo XI. O I é o numeral romano I, o h é de hexagonal e o c é de cúbico - eles representam a estrutura cristalina da água. O gelo comum é o hexagonal, não à tôa os flocos de neve formados na Terra têm padrões hexagoanis (o que não quer dizer que em outros planetas com temperaturas ou pressões mais extremas eles também teriam!)

O gelo XI é uma forma ferroelétrica e ortorrômbica, isto é, um parelelepípedo onde os lados são diferentes, como na figura seguinte:
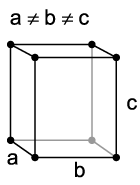
Uma representação do gelo XI, embora seja difícil perceber sua ortorrombicidade é a seguinte:

Cada tipo de gelo tem uma estrutura molecular diferente, e isso afeta várias propriedades, como densidade e constante dielétrica. Por exemplo, não são todos os gelos que flutuam em água, o gelo X, por exemplo, tem densidade 2,51 g/cm³, para se ter uma idéia a densidade do alumínio é de 2,70 g/cm³, mas gelos como o X só se formam a pressões acima de 10^8 Pa, umas 1000 atmosferas. E apesar de o mapa só ir até XII, já se aconhece até o gelo XIV, e sabe-se lá se não vão acabar topando com mais algum.
Já o gelo amorfo não aparece no diagrama porque ele só se forma sob condições extremas: Uma queda de temperatura velocíssima da água líqüida, por volta de 1 000 000 K/s (é claro que o resfriamento vai durar bem menos do que 1 segundo, para não termos que aquecer a água até um milhão Kelvin.) Nessas cicunstâncias não haverá tempo para os cristais de gelo se formarem e teremos uma estrutura amorfa toda bagunçada, como um vidro. O que define um objeto como sólido é a presença de estrutura cristalina, então nesse sentido o gelo amorfo é um líqüido (se bem que muita gente prefere dizer que é simplesmente um sólido amorfo.)
Referências:
http://en.wikipedia.org/wiki/Icehttp://www.lsbu.ac.uk/water/phase.htmlhttp://wine1.sb.fsu.edu/chm1045/notes/Forces/Phase/Forces06.htm